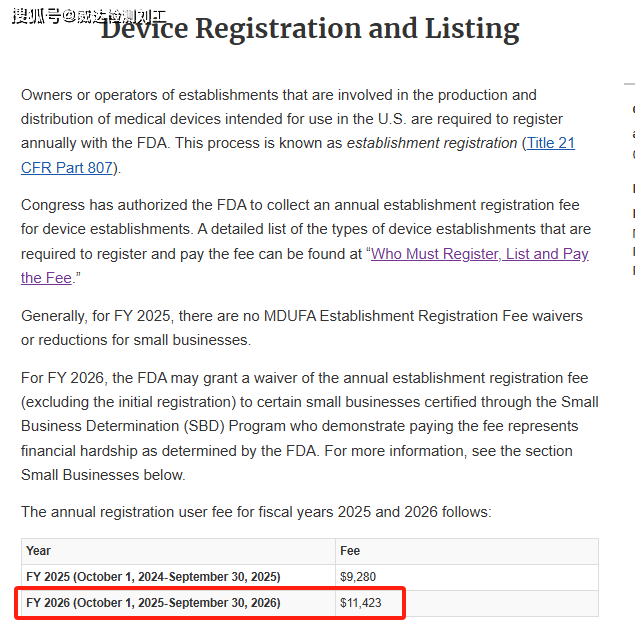
澳门新莆京,澳门新莆京娱乐网站,澳门新莆京注册,澳门新莆京app下载,真人视讯,棋牌游戏平台,澳门博彩。澳门新莆京娱乐网站为广大用户提供真人视讯、棋牌游戏、电子游艺等高端娱乐服务,注册送88元体验金,安全稳定,支持APP下载,海量游戏全天开放,尽享澳门级娱乐体验。2025年7月30日,FDA公布2026年美国FDA医疗器械企业年费,2026年企业年费为为USD11423, 较2025年USD9280, 增涨了USD 2143, 上涨了23%。无形中增加了中国企业进入美国市场的成本, 提高了中国企业进入美国市场的门槛。
I类:低风险(如绷带、牙刷),通常豁免510(k),需完成企业注册和产品列名。
II类:中等风险(如血糖仪、超声设备),需提交510(k)申请,证明与已上市器械实质等同。
III类:高风险(如心脏起搏器、人工关节),需通过PMA(上市前批准),提交临床试验数据及设计验证文件。
510(k):适用于II类器械,需提供技术文件、性能测试报告及对比分析。
建立符合ISO 13485或FDA QSR(质量系统规范)的质量管理体系,涵盖质量控制、记录管理及追溯能力。
生产设施需通过FDA现场检查,确保卫生条件、设备工艺及生产流程符合标准。
产品需全面符合FDA法规要求,包括成分安全性、生产工艺合理性、标签规范性及包装适用性。
b,小型企业(年收入少于1,000,000)可申请减免,费用减半至6,216。
10月1日之前办理的注册,需在当年10月至12月内完成缴费续签;10月1日之后办理的注册,需在下一年的10月至12月内完成缴费续签。


